Бензиловый спирт — это самый простой и наиболее важный промышленный ароматический спирт с химической формулой C6H5CH2OH. Это бесцветная жидкость комнатной температуры со слабым приятным запахом, слабо растворимая в воде, но смешивающаяся со многими органическими растворителями.
Впервые бензиловый спирт был получен из масла горького миндаля Либихом и Велером в 1832 году. Канниццаро определил его структуру в 1853 году, используя одноименную реакцию, в которой бензальдегид непропорционально превращается в бензойную кислоту и бензиловый спирт под действием щелочи.
Бензиловый спирт встречается в природе как в свободной форме, так и в виде сложных эфиров, таких как эфиры уксусной, бензойной, салициловой и коричной кислот. Он содержится в бальзамах Перу и Толу, маслах гиацинта и желтофиоли, масле иланг-иланга и других эфирных маслах. Он также содержится в виде глюкозида в кукурузе.
Содержание
1. Физические свойства бензилового спирта
Бензиловый спирт представляет собой бесцветную жидкость со слабым ароматическим запахом и слегка раздражающим действием на слизистые оболочки. Он плохо растворяется со многими органическими растворителями.
В следующей таблице представлены некоторые физические свойства бензилового спирта:
| Свойство | Значение |
|---|---|
| Молекулярная формула | C7H8O |
| Молекулярная масса | 108,14 г/моль |
| Температура кипения | 205,4 °C при давлении 101,3 кПа |
| Температура плавления | -15,4 °C |
| Показатель преломления | 1,5400 |
| Плотность | 1,061 г/см3 при 0 °C |
| Удельная теплоемкость | 1972 Дж/кг·К при 20 °C |
| Теплота плавления | 82,9 Дж/г |
| Теплота испарения | 467,0 Дж/г при 205,4 °C |
| Стандартная энтальпия горения | 34,58 кДж/г |
| Температура вспышки | 101 °C |
| Температура самовоспламенения | 435 °C |
| Нижний предел взрываемости | 1,3 об. % при температуре 170 °C и давлении 101,3 кПа |
| Верхний предел взрываемости | 13,0 об. % |
| Растворимость в воде | 4,0 г/100 г при 20 °C |
| Растворимость воды в бензиловом спирте | 5,1 г/100 г при 20 °C |
| Динамическая вязкость | 5,584×10-3 Па·с при 20 °C |
| Поверхностное натяжение | 39,96×10-3 Н/м при 20 °C |
| Дипольный момент | 5,571×10-30 C·м (1,67 D) |
| Относительная диэлектрическая проницаемость | 11,92 при 30 °C |
| Относительная диэлектрическая проницаемость | 9,81 при 60 °C |
2. Химические реакции бензилового спирта
Уникальные свойства бензилового спирта в первую очередь обусловлены его гидроксильной группой, которая ведет себя подобно таковой у алифатических спиртов. Однако близость к ароматическому кольцу делает его более реакционноспособным. Бензиловый спирт менее кислый, чем изомерные крезолы, поэтому он не полностью растворяется в водных щелочах.
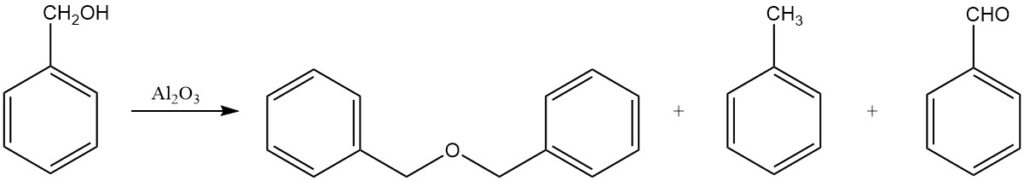
При нагревании с дегидратирующими агентами, такими как оксид алюминия, бензиловый спирт образует различные соединения, включая дибензиловый эфир, толуол и бензальдегид. Дибензиловый эфир также может быть получен взаимодействием бензилового спирта с алкилгалогенидами в присутствии бис (ацетилацетонато) никеля в качестве катализатора.
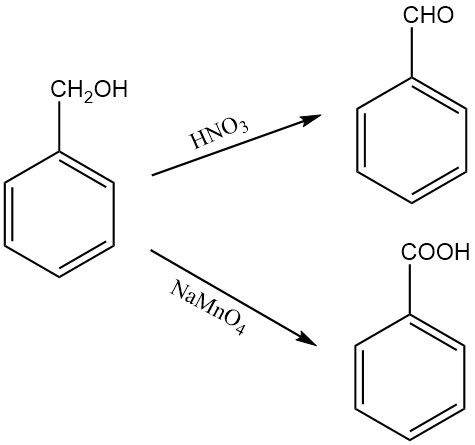
При окислении бензилового спирта образуется бензальдегид или бензойная кислота, в зависимости от окислителя и условий реакции. Например, азотная кислота окисляет бензиловый спирт до бензальдегида, в то время как твердый моногидрат перманганата натрия окисляет его до бензойной кислоты.
Бензиловый спирт также может окисляться до бензальдегида в условиях окисления по Оппенауэру с использованием фурфурола в качестве акцептора водорода. Воздействие воздуха может постепенно окислять бензиловый спирт до бензальдегида.
При дегидрировании бензилового спирта в газовой фазе с использованием катализаторов из меди или благородных металлов также образуется бензальдегид в качестве основного продукта.
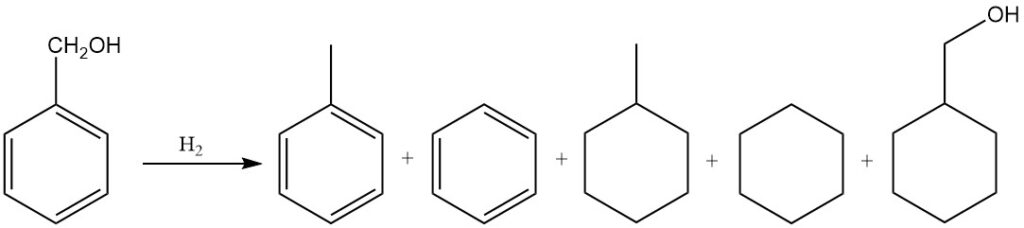
При гидрировании бензилового спирта в различных условиях можно получать различные продукты, включая толуол, бензол, метилциклогексан, циклогексан и гидроксиметилциклогексан. Бензиловый спирт также вступает в реакцию с галогенидами водорода с образованием соответствующих бензилгалогенидов.
Кроме того, бензиловый спирт может быть преобразован в бензоилхлорид при хлорировании боковых цепей ароматических соединений. Он также может быть преобразован в различные алкиламины при взаимодействии с аммиаком или аминами.
Катализаторы Фриделя-Крафтса могут быть использованы для алкилирования бензилового спирта. Например, при взаимодействии бензилового спирта с бензолом образуется дифенилметан, а при взаимодействии его с фенолом образуется смесь 2- и 4-бензилфенолов.
Бензиловый спирт реагирует с органическими и неорганическими кислотами, галогенидами кислот или ангидридами кислот с образованием сложных эфиров. При кислотно-катализируемых реакциях с альдегидами образуются ацетали. Кроме того, при взаимодействии бензилового спирта с монооксидом углерода в присутствии карбонильных катализаторов образуется фенилуксусная кислота.
Обработка бензилового спирта определенными катализаторами, такими как безводный хлорид алюминия или хлорид цинка, удаляет воду с образованием смолистых продуктов. Даже небольшие количества бромистого водорода и железа (II) могут инициировать экзотермическую реакцию поликонденсации бензилового спирта при температурах выше 150 °C.
Эта реакция может повысить температуру до 240 °C и вызвать внезапный скачок давления в закрытом сосуде. Поэтому рекомендуется не нагревать бензиловый спирт выше 100 °C, если только в нем нет кислотных примесей и растворенного железа.
3. Производство бензилового спирта
Существует только два промышленно важных метода получения бензилового спирта:
- Гидролиз бензилхлорида
- Гидрирование бензальдегида
3.1. Получение бензилового спирта гидролизом бензилхлорида
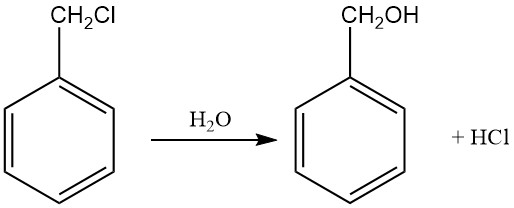
Гидролиз бензилхлорида является обратимой реакцией, которую можно осуществить практически количественно в присутствии основных омыляющих агентов, нейтрализующих соляную кислоту, образующуюся в качестве побочного продукта.
Реакцию обычно проводят путем нагревания бензилхлорида с избытком водного раствора оксида, гидроксида или карбоната щелочного или щелочноземельного металла. Предпочтительным омылителем является сода.
Для производства бензилового спирта в промышленных масштабах обычно используется следующая процедура:
- 126,5 частей бензилхлорида добавляют к 610 частям кипящего 10%-ного раствора соды при перемешивании.
- Реакционную смесь кипятят с обратным холодильником и перемешивают до тех пор, пока не перестанет выделяться углекислый газ (это занимает около 5-6 часов).
- Реакционную смесь охлаждают и удаляют верхний слой, состоящий из неочищенного бензилового спирта.
- Приведенный ниже раствор хлорида натрия экстрагируется органическим сольвентом, таким как бензол или толуол, для извлечения любого растворенного бензилового спирта.
- Неочищенный бензиловый спирт очищают фракционной перегонкой при пониженном давлении для получения чистого продукта.
Выход бензилового спирта в результате этого процесса составляет 67%, а дибензилового эфира — 8%.
Для сокращения времени реакции конечный остаток бензилхлорида можно гидролизовать раствором гидроксида натрия после 3-часового омыления раствором соды. Это сокращает общее время омыления до 4 часов.
Процентное содержание образующегося в реакции дибензилового эфира можно снизить, используя инертный растворитель, такой как бензол, толуол или ксилол, или путем гидролиза бензилхлорида в непрерывном процессе.
В новом непрерывном процессе бензилхлорид и щелочной омыляющий агент взаимодействуют в противотоках в инертном органическом растворителе в проточном реакторе. Спирт экстрагируется из водной щелочной фазы инертным органическим растворителем в зоне экстракции.
Затем неочищенный бензиловый спирт промывается водой в зоне промывки. Проточный реактор, зона экстракции и зона промывки объединены в специальное устройство. Этот процесс может осуществляться при низких температурах реакции (120-150 °C) и с небольшим стехиометрическим избытком омыляющего агента (5-25%).
Также были разработаны двухстадийные способы получения бензилового спирта, но они не приобрели большого коммерческого значения.
3.2. Получение бензилового спирта путем гидрирования и восстановления бензальдегида
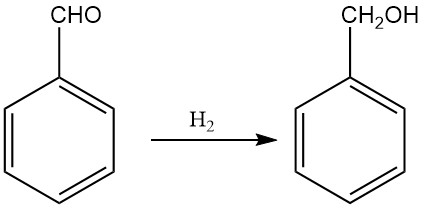
Промышленное производство бензилового спирта путем гидрирования бензальдегида приобрело важное значение из-за большого количества бензальдегида, доступного в качестве побочного продукта процесса Dow для производства фенола и процесса Snia Viscosa для производства капролактама.
В зависимости от условий реакции бензальдегид может быть гидрирован с образованием различных продуктов, включая бензиловый спирт, толуол, гидроксиметилциклогексан и метилциклогексан. Однако высокие выходы бензилового спирта можно получить, регулируя условия реакции и катализаторы.
Подходящие катализаторы для гидрирования бензальдегида включают:
- Никель Ранея, легированный переходными металлами
- Никель или платиновые металлы с фосфинами или фосфиноксидами
- Палладий в сочетании с органическим азотом, щелочным основанием, водой или другим переходным металлом
Когда бензальдегид гидрируют при температуре 70-200 °C и давлении водорода 1-4 МПа, за короткое время реакции получают высокие выходы бензилового спирта.
В хорошо известном непрерывном процессе используется катализатор из платины, оксида алюминия и оксида лития для эффективного и селективного гидрирования бензальдегида в бензиловый спирт.
Другие методы с использованием восстановителей, таких как станнан, гидрид натрия, цинк или микроорганизмы, не имеют промышленного значения.
Реакция Канниццаро больше не используется в промышленности для получения бензилового спирта.
3.3. Получение бензилового спирта окислением толуола
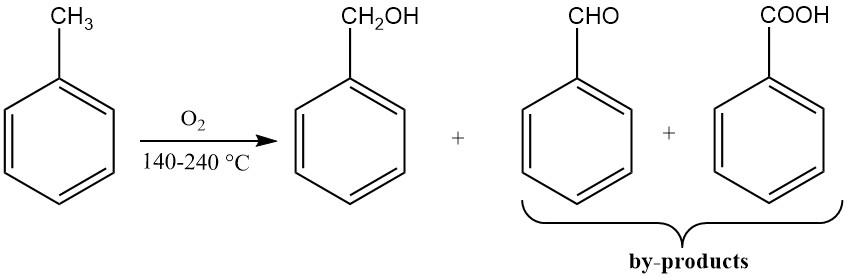
Каталитическое окисление толуола приводит к низкому выходу бензилового спирта, поскольку условия реакции благоприятствуют дальнейшему окислению до бензальдегида и бензойной кислоты. В большинстве процессов производства бензилового спирта с использованием толуола в качестве сырья выделяются промежуточные побочные продукты.
Один из способов заключается в окислении толуола обедненным кислородом воздухом при температуре 170-220 °C и достаточном давлении для поддержания реакционной среды жидкой. Эту реакцию проводят в присутствии стабилизаторов органических гидропероксидов, таких как пирофосфат натрия или фторид натрия.
Если допустить реакцию не более 10% толуола, основным продуктом будет гидропероксид бензила. Последующее разложение гидропероксида бензила при температуре 165 °C в присутствии растворимых солей кобальта приводит к образованию бензилового спирта.
Бензальдегид и бензойная кислота образуются в качестве побочных продуктов. Гидропероксид бензила также можно восстановить до бензилового спирта с помощью сульфитов щелочных металлов.
Другой процесс заключается в окислении толуола на воздухе до жидкой фазы в присутствии кислот, хлоридов кислот или ангидридов кислот. При этом образуются бензиловые эфиры этих кислот, которые затем могут быть омылены с образованием бензилового спирта.
Например, при окислении толуола в присутствии уксусного ангидрида при 140-240 °C и 1-3 МПа образуется бензилацетат. Окисление прекращают после того, как вступит в реакцию 10% толуола. После омыления продукта окисления из 500 г прореагировавшего толуола можно получить 350 г бензилового спирта, 55 г бензальдегида и 67 г бензойной кислоты.
Фенольные примеси, такие как крезолы, неизбежно присутствуют в бензиловом спирте, получаемом окислением толуола. Эти примеси можно удалить путем промывки паров бензилового спирта противотоком раствора бензилата щелочи в пластинчатой колонне или насадочной колонне.
3.4. Другие производственные процессы
Гидрирование сложных эфиров бензойной кислоты с образованием бензилового спирта является привлекательным методом, когда сложные эфиры бензойной кислоты образуются в больших количествах, например, при производстве диметилтерефталата по процессу Виттена.
Для этой реакции предпочтительны медные катализаторы. Сложные эфиры бензойной кислоты могут быть гидрированы до бензилового спирта с использованием медного катализатора, нанесенного на оксиды щелочноземельных элементов или карбонаты. Селективность может быть улучшена добавлением хрома в катализатор. Реакцию обычно проводят при температурах 100-300°C и давлении выше 6 МПа.
Другие катализаторы гидрирования сложных эфиров бензойной кислоты до бензилового спирта включают рутений, родий, платину и палладий, активируемые аренами, кетилами или алкоксидами щелочных металлов. Эти катализаторы позволяют проводить реакцию в мягких условиях с высокой селективностью.
Трехстадийные процессы получения бензилового спирта из толуола обычно включают гидрирование метилбензоата в присутствии медно-хромового катализатора:
- Окисление толуола до бензойной кислоты
- Этерификация метанолом
- Гидрирование метилбензоата до бензилового спирта
Этот процесс позволяет получать бензиловый спирт при очень низких затратах.
Другие процессы, включая гидрирование или электрохимическое восстановление бензойной кислоты, гидролиз бензилсульфоновой кислоты и декарбоксилирование бензилформиата, не важны для промышленного производства бензилового спирта, но их можно использовать для получения производных, замещенных в ароматическом кольце.
Бензиловый спирт также может быть получен из бензилбензоата, который образуется как побочный продукт производства бензойной кислоты.
4. Применение бензилового спирта
Бензиловый спирт является хорошим растворителем для поверхностных покрытий, смол, сложных эфиров целлюлозы, простых эфиров, алкидных смол, акриловых смол и жиров. Он также используется в чернилах для шариковых ручек, для улучшения текучести и блеска поверхностных покрытий, а также в качестве вспомогательного средства при окрашивании шерсти, полиамидов и сложных полиэфиров.
Поскольку он имеет слабый запах, его используют в качестве растворителя и разбавителя в парфюмерии и ароматизаторах.
Бензиловый спирт также используется в качестве ускорителя проявки в цветной фотографии.
Он используется в качестве местного анестетика в фармацевтике, а также в качестве ингредиента мазей и других препаратов благодаря своему бактерицидному действию.
Бензиловый спирт является исходным материалом для получения многих бензиловых эфиров, которые используются в качестве отдушек, ароматизаторов, стабилизаторов летучих отдушек и пластификаторов.
Он также используется при экстрактивной перегонке м- и п-ксилолов и м- и п-крезолов.
Другие виды применения бензилового спирта включают:
- Растворитель для очистки и обезжиривания
- Присадка к топливу
- Ингредиент средства личной гигиены (например, шампуня, кондиционера, зубной пасты)
- Фармацевтический наполнитель (например, консервант, солюбилизатор)
- Сельскохозяйственный химикат (например, митицид, инсектицид)
5. Токсикология бензилового спирта
Бензиловый спирт — универсальный отдушка, консервант и противомикробное средство, используемое в фармацевтике, мыле, моющих средствах, косметике и пищевых продуктах. Управление по контролю за продуктами питания и лекарствами США “в целом считает его безопасным” (GRAS), но пределы воздействия на окружающую среду или рабочее место еще не установлены.
Бензиловый спирт умеренно токсичен, при остром приеме внутрь значения LD50 составляют 1,2 г / кг у крыс и 1,6 г / кг у мышей. Он также может всасываться через кожу в токсичных количествах, при этом дермальный LD50 у морских свинок составляет менее 5 мл / кг.
Бензиловый спирт не классифицируется как канцероген, и нет данных о его тератогенном или репродуктивном действии. Однако важно отметить, что бензиловый спирт высокотоксичен для новорожденных людей, причем предполагаемая смертельная доза значительно ниже, чем у взрослых.
Бензиловый спирт широко используется в качестве консерванта при внутривенном введении лекарственных растворов, но требуется осторожность из-за его высокой токсичности для новорожденных.
Бензиловый спирт также сильно токсичен и вызывает раздражение глаз и может вызывать легкое или умеренное раздражение кожи. У некоторых людей могут возникать реакции гиперчувствительности к бензиловому спирту, как при местном, так и при парентеральном введении.
Симптомы интоксикации бензиловым спиртом включают рвоту, диарею, угнетение центральной нервной системы, возбудимость, паралич мышц, судороги, нарушение дыхания и коллапс.
Для снижения воздействия бензилового спирта важно использовать соответствующие системы вентиляции, автономное дыхательное оборудование, защитные очки, перчатки и спецодежду.
Ссылка
- Бензиловый спирт; Энциклопедия промышленной химии Ульмана. – https://onlinelibrary.wiley.com/doi/10.1002/14356007.a04_001

